️ Chẩn đoán và điều trị ung thư phổi
1. ĐẠI CƯƠNG
1.1. KHÁI NIỆM
Ung thư phổi là bệnh xuất hiện một khối u ác tính do sự tăng sinh tế bào không thể kiểm soát trong các mô phổi. Sự tăng sinh tế bào này có thể lan ra ngoài phổi đến các mô hoặc bộ phận khác của cơ thể gọi là di căn.
Hầu hết các loại ung thư bắt nguồn từ trong phổi (ung thư phổi nguyên phát) là ung thư biểu mô. Ung thư phổi được chia làm hai loại chính là ung thư phổi tế bào nhỏ (Small Cell Lung Cancer-SCLC) và ung thư phổi không phải tế bào nhỏ (Non-Small Cell Lung Cancer-NSCLC). Triệu chứng phổ biến nhất của căn bệnh này là ho (bao gồm cả ho ra máu), sụt cân, khó thở, và đau ngực.
Tính trên phạm vi toàn thế giới trong năm 2012, số ca mắc ung thư phổi là 1,8 triệu, trong đó 1,6 triệu người đã tử vong Điều này làm cho ung thư phổi là loại ung thư khiến số nam giới tử vong là cao nhất và số nữ giới tử vong là cao thứ nhì sau ung thư vú. Độ tuổi chẩn đoán thường gặp nhất là 70. Tại Mỹ, 17,4% số bệnh nhân sống sót sau năm năm kể từ thời điểm xác định mắc bệnh, còn đối với những nước đang phát triển kết quả về mặt trung bình kém hơn.
1.2. NGUYÊN NHÂN
1.2.1. Hút thuốc lá
Phần lớn các ca ung thư phổi (85%) có liên quan với hút thuốc lá trong một thời gian dài. Khoảng 10–15% trường hợp còn lại bệnh xảy ra ở những người chưa từng hút thuốc. Đối với những trường hợp này, nguyên nhân được cho là là do sự kết hợp của các tác nhân di truyền, việc tiếp xúc trực tiếp với khí radon, amiăng, hút thuốc thụ động, hay không khí ô nhiễm.
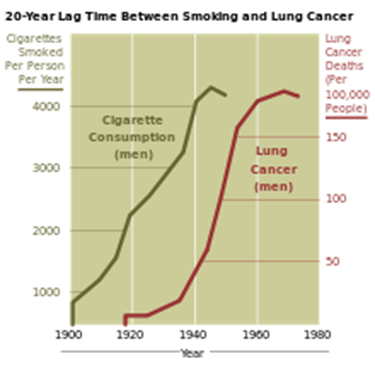
Hình 1. Liên quan giữa ung thư phổi và hút thuốc lá.
Đồ thị cho thấy sự gia tăng về doanh số sản phẩm thuốc lá bán ra tại Mỹ trong bốn thập niên đầu thế kỷ 20 (số điếu thuốc một nam giới một năm) đã dẫn tới sự gia tăng nhanh chóng tương ứng của tỉ lệ số ca mắc ung thư phổi trong các thập niên 1930, 1940 và 1950 (số ca tử vong trên mỗi 100.000 nam giới mỗi năm).
Ung thư phát triển từ tổn thương ADN và những sự biến đổi ngoài di truyền (epigenetic). Những đột biến này ảnh hưởng đến các chức năng bình thường của tế bào, bao gồm sự tăng sinh tế bào, quá trình chết theo chương trình của tế bào (apoptosis) và sửa chữa ADN. Tổn thương tích lũy càng nhiều thì nguy cơ mắc ung thư càng tăng lên.
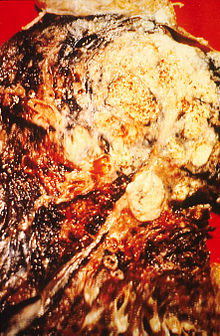
Hình 2. Mặt cắt ngang một lá phổi người: vùng trắng ở thùy trên là khối u ung thư, các vùng có màu đen là do khói thuốc gây ra sự biến đổi màu.
Hút thuốc, đặc biệt là thuốc lá điếu, cho đến nay được coi là tác nhân chính gây ra ung thư phổi. Trong khói thuốc lá có chứa ít nhất 73 chất gây ung thư đã biết, như là benzo(a)pyren, NNK, buta-1,3-dien, và một đồng vị phóng xạ của poloni đó là poloni-210. Tại các nước phát triển, 90% số ca tử vong do ung thư phổi ở nam giới trong năm 2000 được cho là do hút thuốc, tỉ lệ này đối với phụ nữ là 70%. Hút thuốc cũng là nguyên nhân của khoảng 85% số ca mắc bệnh.
Việc hít phải khói thuốc từ một người khác đang hút thuốc, hay thường được gọi là hút thuốc thụ động, là một trong những nguyên nhân gây ra ung thư phổi ở những người không hút thuốc. Các nghiên cứu tới từ Mỹ, châu Âu, và Anh đã cùng nhất quán chỉ ra mức độ gia tăng đáng kể đối với những trường hợp hút thuốc thụ động. Nguy cơ mắc bệnh đối với những người sống cùng với người hút thuốc tăng lên từ 20–30% trong khi đối với những người làm việc trong môi trường có khói thuốc là 16–19%. Các nghiên cứu chỉ ra khói thuốc bay ra ngoài không khí từ điếu thuốc cháy (sidestream smoke) nguy hiểm hơn nhiều so với loại khói mà người hút thuốc trực tiếp hít vào (mainstream smoke).
Khói cần sa cũng chứa nhiều chất gây ung thư tương tự như khói thuốc lá. Tuy nhiên, mối quan hệ giữa việc hút cần sa và nguy cơ mắc ung thư phổi là không rõ ràng. Một cuộc xem xét lại thực hiện năm 2013 đã không tìm thấy sự gia tăng nguy cơ từ việc dùng cần sa ít đến trung bình. Tuy nhiên đợt kiểm tra năm 2014 lại chỉ ra hút cần sa làm tăng gấp đôi nguy cơ mắc ung thư phổi.
1.2.2. Khí Radon
Radon là một loại khí không màu, không mùi được tạo ra từ hoạt động phân rã chất phóng xạ radi là sản phẩm phân rã của urani và được tìm thấy trong lớp vỏ Trái Đất. Các sản phẩm phân rã của quá trình phóng xạ ion hóa vật chất di truyền, gây ra những sự đột biến mà đôi khi chuyển đổi thành ung thư. Tại Mỹ, Radon là nguyên nhân gây ra ung thư phổi phổ biến thứ hai khiến khoảng 21.000 người tử vong mỗi năm. Mức độ tập trung khí Radon tăng lên mỗi 100 Bq/m³ thì nguy cơ mắc bệnh tăng lên từ 8–16%. Hàm lượng khí Radon có sự khác biệt tùy vào khu vực và thành phần đất đá ở dưới mặt đất.
1.2.3. Amiang
Amiăng là loại chất có thể gây ra nhiều loại bệnh ở phổi khác nhau, trong đó có ung thư phổi. Hút thuốc lá và amiăng có ảnh hưởng kết hợp trong việc dẫn tới sự hình thành ung thư phổi. Đối với những người hút thuốc có tiếp xúc với amiăng, nguy cơ mắc bệnh tăng tới 45 lần. Ngoài ra amiăng còn có thể gây ra ung thư màng phổi, được gọi là u trung biểu mô màng phổi (khác với ung thư phổi).
1.2.4. Ô nhiễm không khí
Ô nhiễm không khí ngoài trời có một tác động nhỏ đến sự gia tăng nguy cơ mắc ung thư phổi. Các hạt vật chất nhỏ (bụi PM2.5) và các sol khí sunfat (có trong khí thải xe cộ) có liên quan tới sự gia tăng nhẹ nguy cơ. Lượng nitơ điôxít trong không khí tăng lên 10 phần tỉ sẽ làm tăng nguy cơ mắc bệnh lên 14%. Theo ước tính, ô nhiễm không khí ngoài trời là nguyên nhân của 1–2% số trường hợp mắc ung thư phổi.
Có bằng chứng ủng hộ ô nhiễm không khí trong nhà liên quan tới việc đốt củi, than, phân hay tàn dư thực vật phục vụ cho nấu nướng hay sưởi ấm trong gia đình làm gia tăng nguy cơ mắc ung thư phổi. Phụ nữ tiếp xúc (phơi nhiễm) với khói than trong nhà có nguy cơ gấp đôi và các sản phẩm phụ của việc đốt cháy sinh khối bị nghi ngờ là tác nhân gây ung thư. Nguy cơ này ảnh hưởng đến khoảng 2,4 tỉ người trên toàn cầu và người ta tin rằng nó là nguyên nhân của 1,5% số ca tử vong do ung thư phổi.
1.2.5. Di truyền
Khoảng 8% số ca ung thư phổi có nguyên nhân tới từ các yếu tố di truyền. Một người có quan hệ họ hàng với người bị ung thư phổi thì nguy cơ mắc bệnh sẽ tăng lên 2,4 lần. Điều này khả năng là do sự kết hợp gen. Tính đa hình của các nhiễm sắc thể 5, 6 và 15 có tác động đến nguy cơ mắc ung thư phổi.
1.2.6. Nguyên nhân khác
Ngoài các nguyên nhân kể trên, còn nhiều yếu tố khác có mối liên quan với ung thư phổi, như các chất hóa học, nghề nghiệp, và tình trạng tiếp xúc với môi trường ô nhiễm. Cơ quan Nghiên cứu Ung thư Quốc tế(IARC) nói rằng có "bằng chứng đầy đủ" chỉ ra các yếu tố dưới đây là tác nhân gây ra ung thư ở phổi:
- Một số kim loại (sản phẩm nhôm, cadimi và các hợp chất của cadimi, các hợp chất crom, berili và các hợp chất của berili, sắt và thép nóng chảy, các hợp chất của niken, asen và các hợp chất vô cơ của asen, hematitkhai thác dưới mặt đất).
- Một số sản phẩm cháy không hoàn toàn, than đá (khí thải phát ra trong nhà từ việc đốt than), khí hóa than, dầu nhựa than đá, than cốc, bồ hóng, khí thải động cơ diesel).
- Bức xạ ion hóa (bức xạ tia X, bức xạ gamma, plutoni).
- Một số khí độc (metyl ete dùng trong công nghiệp, Bis-(clorometyl) ete, mù tạc lưu huỳnh, MOPP (hỗn hợp vincristin-prednison-mù tạc nitơ-procarbazin ), hơi sơn).
- Sản phẩm cao su và bụi silic ôxít kết tinh (bụi tinh thể SiO2).
1.3. BỆNH SINH
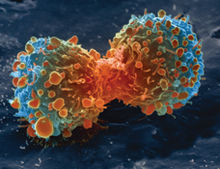
Hình 3. Ảnh màu giả chụp từ kính hiển vi điện tử quét mô tả một tế bào ung thư phổi đang phân chia.
Tương tự như nhiều loại ung thư khác, ung thư phổi bắt nguồn từ sự hoạt hóa các gen gây ung thư(oncogene) hoặc sự bất hoạt các gen ức chế khối u (hay gen chống ung thư, antioncogene). Các tác nhân gây ung thư gây ra đột biến ở những gen này, qua đó mở đường cho sự phát triển của bệnh.
Những đột biến trong gen tiền ung thư (proto-oncogene) K-ras là nguyên nhân của 10–30% số ca ung thư biểu mô tuyến phổi. Khoảng 4% số trường hợp ung thư phổi không phải tế bào nhỏ có liên quan tới gen tổ hợp tyrosine kinase EML4-ALK.
Những đột biến ngoài di truyền (epigenetic) như sự biến đổi quá trình metyl hóa ADN, sự sửa đổi đuôi histon, hay sự điều chỉnh microARN, có thể làm cho các gen ức chế khối u ngừng hoạt động.
Thụ thể yếu tố tăng trưởng thượng bì (EGFR) điều chỉnh quá trình tăng sinh tế bào, quá trình chết theo chương trình của tế bào (apoptosis), tân tạo mạch (angiogenesis), và sự xâm lấn của khối u. Những đột biến và khuếch đại EGFR thường gặp ở ung thư phổi không phải tế bào nhỏ cung cấp cơ sở cho việc điều trị bằng các chất ức chế EGFR. Thụ thể HER2/neu ít bị ảnh hưởng. Các gen thường bị đột biến hay khuếch đại khác là c-MET, NKX2-1, LKB1, PIK3CA, và BRAF.
Cho tới nay người ta chưa hiểu biết hết về các dòng tế bào gốc. Cơ chế có thể liên quan tới sự hoạt hóa một cách bất thường các tế bào gốc. Trong đường thở gần (hay đường dẫn khí, khí quản), các tế bào gốc biểu hiện keratin 5 nhiều khả năng bị tác động và thường dẫn tới ung thư phổi tế bào vảy (ung thư biểu mô tế bào vảy của phổi). Trong đường thở giữa, các tế bào gốc liên quan bao gồm tế bào club (ban đầu được biết đến với tên gọi tế bào Clara) và tế bào biểu mô thần kinh biểu lộ protein chế tiết của tế bào club. Ung thư phổi tế bào nhỏ có thể có nguồn gốc từ những dòng tế bào này hoặc tế bào thần kinh nội tiết, và có thể biểu hiện glycoprotein CD44.
Di căn của ung thư phổi đòi hỏi quá trình chuyển đổi kiểu tế bào từ biểu mô thành trung mô. Điều này có thể xảy ra thông qua sự hoạt hóa các đường truyền tín hiệu như Akt/GSK3Beta, MEK-ERK, Fas, và Par6.
2. LÂM SÀNG VÀ CẬN LÂM SÀNG
2.1. Lâm sàng
- Những dấu hiệu và triệu chứng nghi ngờ ung thư phổi bao gồm:
- Triệu chứng về đường hô hấp: ho, ho ra máu, thở khò khè, khó thở.
- Triệu chứng toàn thân: sụt cân, mệt mỏi, sốt, ngón tay dùi trống.
- Triệu chứng do ung thư chèn ép nhiều sang các cơ quan kề bên: đau ngực, đau xương, tắc nghẽn tĩnh mạch chủ trên, khó nuốt
Nếu ung thư phát triển ở phế quản, có thể cản trở dòng khí lưu thông, gây ra khó thở. Sự cản trở này có thể dẫn tới việc tích lũy chất bài tiết phía sau chỗ tắc là điều kiện gây viêm phổi.
Tùy thuộc vào loại khối u, hội chứng cận ung thư (paraneoplastic syndrome) có thể là dấu hiệu ban đầu của bệnh. Những triệu chứng này có thể bao gồm tăng canxi máu, hội chứng tăng tiết hormone chống bài niệu không phù hợp (SIADH, nước tiếu đậm đặc và máu loãng một cách bất thường), tăng hormon vỏ thượng thận (ACTH), hội chứng nhược cơ Lambert–Eaton (cơ yếu đi do rối loạn tự miễn dịch).
Các khối u trên đỉnh phổi, với tên gọi khối u Pancoast, có thể xâm lấn hệ thần kinh giao cảm, dẫn tới hội chứng horner (sụp mí mắt và co đồng tử cùng bên) và gây tổn thương đám rối thần kinh cánh tay (brachial plexus).
Phần lớn các triệu chứng của ung thư phổi (chán ăn, sụt cân, sốt, mệt mỏi) là không đặc hiệu. Đối với nhiều người, vào thời điểm phát hiện ra những dấu hiệu bệnh và đi khám, khối u đã di căn ra ngoài vị trí khởi phát. Các triệu chứng có thể báo hiệu quá trình di căn đã xuất hiện bao gồm sụt cân, đau xương và các triệu chứng về thần kinh (đau đầu, ngất xỉu, co giật, yếu chi). Những vị trí khối u lan tới thường gặp là não, xương, tuyến thượng thận, bên phổi còn lại, gan, màng ngoài tim, và thận. Khoảng 10% số ca ung thư phổi không thấy triệu chứng khi chẩn đoán, những trường hợp này bệnh tình cờ được phát hiện nhờ việc chụp X quang ngực định kỳ.
- Các giai đoạn của ung thư phổi không phải tế bào nhỏ:
- Giai đoạn I. Ung thư ở giai đoạn này đã xâm chiếm các mô phổi nằm bên dưới nhưng chưa lan đến các hạch bạch huyết.
- Giai đoạn II. Ung thư đã lan đến hạch bạch huyết lân cận hoặc cấu trúc thành ngực hoặc các tổ chức lân cận khác.
- Giai đoạn IIIA. Ở giai đoạn này, ung thư đã lan rộng từ phổi đến các hạch bạch huyết ở trung thất.
- Giai đoạn IIIB. Ung thư đã lan đến các tạng khác trong lồng ngực như tim, mạch máu, khí quản và thực quản (tất cả chỉ trong lồng ngực) hoặc đến các hạch bạch huyết khu vực xương đòn hoặc đến các mô bao quanh phổi trong lồng ngực (màng phổi).
- Giai đoạn IV. Ung thư đã lan ra các phần khác của cơ thể ngoài lồng ngực, chẳng hạn như, gan, xương hay não.
- Các giai đoạn của ung thư phổi:
- Hạn chế. Ung thư giới hạn ở một phổi và các hạch bạch huyết lân cận.
- Lan rộng. Ung thư đã lan ra ngoài một phổi và các hạch bạch huyết gần đó, và có thể đã xâm chiếm cả hai phổi, nhiều hạch bạch huyết từ xa, hoặc các cơ quan khác, chẳng hạn như gan hay não.
2.2. Cận Lâm sàng
2.2.1. X-quang phổi
Ung thư phổi có thể phát hiện qua hình ảnh X-quang phổi và chụp cắt lớp vi tính (CT).
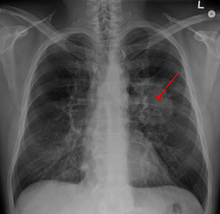
Hình 4. X quang chụp lồng ngực cho thấy một khối u trong phổi (mũi tên).
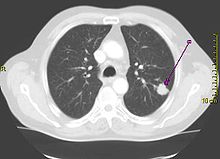
Hình 5. Hình ảnh CT cho thấy một khối u ung thư ở phổi trái (mũi tên).
X-quang phổi có thể cho thấy trung thất rộng ra, tình trạng xẹp phổi, viêm phổi hoặc tràn dịch màng phổi.
Ảnh chụp cắt lớp vi tính (CT) thường được sử dụng để cung cấp thêm thông tin về loại bệnh và mức độ bệnh. Ung thư phổi thường xuất hiện với hình ảnh một nốt đậm đặc cản quang phổi đơn độc (SPN) trên ảnh X quang chụp lồng ngực. Tuy nhiên, chẩn đoán phân biệt là rộng. Dấu hiệu này cũng có ở nhiều loại bệnh khác như lao, nhiễm nấm, ung thư di căn hay viêm phổi tổ chức hóa. Ngoài ra còn các nguyên nhân ít gặp hơn cũng làm xuất hiện nốt đơn độc ở phổi là u mô thừa, nang phế quản, u tuyến, dị dạng động tĩnh mạch, phổi biệt lập, nốt thấp, granulomatosis với polyangiitis (trước đây gọi là u hạt wegener), hoặc lymphoma (u lympho hay ung thư hạch bạch huyết). Ung thư phổi còn có thể được phát hiện một cách tình cờ (incidentaloma) nhờ quan sát thấy hình ảnh nốt phổi đơn độc trên ảnh X quang lồng ngực hoặc ảnh chụp cắt lớp vi tính thực hiện vì một lý do không liên quan. Chẩn đoán xác định ung thư phổi dựa trên kết quả kiểm tra các mô nghi ngờ.
Cần giám sát nốt phổi thường xuyên. Không nên lạm dụng việc chụp CT lâu dài hoặc thường xuyên vì kéo dài thời hạn và mức độ sẽ làm tăng phơi nhiễm với bức xạ.
2.2.2. Sinh thiết phổi
Chẩn đoán xác định phải làm sinh thiết và thường được thực hiện bằng nội soi phế quản hay theo chỉ dẫn của chụp cắt lớp. Nội soi phế quản hoặc làm sinh thiết theo chỉ dẫn CT thường được dùng để lấy mẫu khối u phục vụ cho việc khám nghiệm mô (mô bệnh học).
2.3. Chẩn đoán
Chụp lồng ngực bằng tia X là bước khảo sát đầu tiên nếu người bệnh thông báo các triệu chứng có thể là của ung thư phổi.
Kết quả mô bệnh học qua sinh thiết khối u cho chẩn đoán xác định.
3. PHÂN LOẠI
Ung thư phổi được phân loại dựa theo kết quả xét nghiệm mô bệnh học. Phân loại này quan trọng cho việc theo dõi, điều trị và dự đoán tiên lượng bệnh. Các loại ung thư phổi là ung thư biểu mô, những khối u ác tính phát sinh từ tế bào biểu mô. Ung thư biểu mô phổi được phân theo kích cỡ và diện mạo của các tế bào ác tính quan sát thấy dưới kính hiển vi. Để phục vụ cho mục đích điều trị, người ta phân ra hai loại lớn: ung thư phổi không phải tế bào nhỏ và ung thư phổi tế bào nhỏ.
3.1. Ung thư phổi không phải tế bào nhỏ
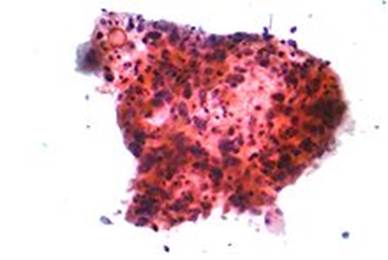
Hình 6. Hình ảnh của ung thư biểu mô tế bào vảy, một loại ung thư không phải tế bào nhỏ, mẫu FNA, nhuộm Papanicolaou.
Ung thư phổi không phải tế bào nhỏ (NSCLC) được chia thành các loại nhỏ hơn, ba loại chính trong đó là:
- Ung thư biểu mô tuyến.
- Ung thư biểu mô tế bào vảy.
- Ung thư biểu mô tế bào lớn.
Gần 40% số ca ung thư phổi là ung thư biểu mô tuyến, loại này thường bắt nguồn từ mô phổi ngoại vi. Mặc dù hầu hết các ca ung thư biểu mô tuyến có liên quan tới việc hút thuốc, nhưng đây cũng là hình thái ung thư phổ biến nhất ở những người hút ít hơn 100 điếu thuốc trong suốt cuộc đời (những người không hút thuốc) và những người có tiền sử hút thuốc khiêm tốn. Một phân loại phụ của ung thư biểu mô tuyến, AIS (tạm dịch: Ung thư biểu mô tuyến phổi tại chỗ, trước đây gọi là ung thư biểu mô bronchioloalveolar), thường gặp hơn ở những nữ giới không hút thuốc và có thể khả năng sống sót về lâu dài là cao hơn.
Ung thư biểu mô tế bào vảy chiếm khoảng 30% số trường hợp ung thư phổi. Loại này thường xảy ra ở gần đường dẫn khí lớn. Một khoảng trống và ổ hoại tử tế bào thường được tìm thấy ở trung tâm khối u.
Khoảng 9% số ca ung thư phổi thuộc loại ung thư biểu mô tế bào lớn. Sở dĩ tên gọi như vậy vì tế bào ung thư là lớn, với sự dư thừa tế bào chất, nhân tế bào lớn và hạch nhân dễ thấy.
3.2. Ung thư phổi tế bào nhỏ
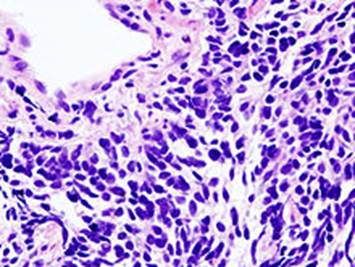
Hình 7. Ung thư phổi tế bào nhỏ (quan sát một mẫu sinh thiết kim lõi qua kính hiển vi).
Ở ung thư phổi tế bào nhỏ (SCLC), các tế bào chứa dày đặc các hạt tiết thể dịch thần kinh (các túi tiết chứa hormon thần kinh nội tiết), do đó khối u loại này có liên đới với hội chứng cận ung thư/nội tiết. Đa số trường hợp bệnh phát sinh ở đường dẫn khí lớn (phế quản chính và phế quản thùy). 60 đến 70% trường hợp bệnh đã lan rộng (không thể xạ trị tại một phạm vi đơn lẻ) tại thời điểm quan sát.
3.3. Loại khác
Có bốn loại phụ được công nhận, mặc dù một số trường hợp có thể bao hàm sự kết hợp của các loại phụ khác nhau. Các loại phụ (hiếm gặp) gồm có:
- Ung thư biểu mô tuyến vảy.
- U carcinoid
- Ung thư biểu mô tuyến phế quản
- Ung thư biểu mô sarcomatoid.
3.4. Ung thư phổi thứ phát (di căn phổi)
Phổi là nơi thường bị các khối u từ các bộ phận khác của cơ thể di căn tới. Ung thư thứ phát được phân loại dựa theo vị trí khối u phát sinh ban đầu, ví dụ: ung thư vú di căn sang phổi được gọi là ung thư vú di căn phổi. Khối u di căn thường có hình tròn trên ảnh X quang.
Ung thư phổi nguyên phát hay di căn tới não, xương, gan, và tuyến thượng thận. Nhuộm miễn dịch(immunostaining) một mẫu sinh thiết thường giúp ích cho việc xác định nguồn gốc khối u. Sự có mặt của các loại protein Napsin-A, TTF-1, CK7 và CK20 giúp xác định loại ung thư phổi. Ung thư phổi tế bào nhỏ có nguồn gốc từ các tế bào thần kinh nội tiết có thể biểu hiện CD56, phân tử kết dính tế bào thần kinh, synaptophysin hoặc chromogranin.
4. ĐIỀU TRỊ VÀ DỰ PHÒNG
Điều trị và kết quả lâu dài phụ thuộc vào loại ung thư, giai đoạn bệnh (mức độ di căn của khối u), và sức khỏe của người bệnh. Đa số trường hợp là không thể chữa khỏi. Các phương pháp chữa trị phổ biến gồm có phẫu thuật, hóa trị và xạ trị. Ung thư phổi không phải tế bào nhỏ đôi khi áp dụng phương pháp phẫu thuật, còn với ung thư phổi tế bào nhỏ thì hóa trị và xạ trị thường đạt hiệu quả tốt hơn.
4.1. Phẫu thuật
Cắt bỏ để loại bỏ một phần nhỏ của phổi có khối u cùng với mô khỏe mạnh ở ranh giới. Cắt bỏ phân đoạn để loại bỏ phần lớn phổi, nhưng không phải là toàn bộ thùy. Cắt thùy để loại bỏ toàn bộ một thùy phổi. Cắt bỏ để loại bỏ toàn bộ một phổi.
Qua phẫu thuật, cũng có thể loại bỏ các hạch bạch huyết ở ngực.
Ung thư phổi khi phẫu thuật có một số rủi ro, bao gồm chảy máu và nhiễm trùng. Mô phổi sẽ nở rộng theo thời gian và làm cho thở dễ dàng hơn. Cần hướng dẫn các bài tập thở để hỗ trợ phục hồi sau phẫu thuật.
4.2. Hóa trị
Hóa trị có thể được sử dụng như biện pháp đầu tiên cho điều trị ung thư phổi hoặc điều trị bổ sung sau khi phẫu thuật. Trong một số trường hợp, hóa trị có thể được sử dụng để làm giảm triệu chứng của bệnh ung thư.
4.3. Xạ trị
Liệu pháp xạ trị có thể được sử dụng một đơn độc hoặc phối hợp với phương pháp điều trị ung thư phổi khác. Đôi khi dùng đồng thời với hóa trị.
4.4. Thuốc điều trị mục tiêu
Phương pháp mới: điều trị mục tiêu là nhắm vào một mục tiêu cụ thể ở các tế bào ung thư. Tùy chọn mục tiêu điều trị để điều trị ung thư phổi bao gồm:
- Bevacizumab (Avastin). Bevacizumab ức chế tăng sinh mạch máu làm dừng phát triển khối u từ việc dừng nguồn cung cấp máu. Mạch máu kết nối với các khối u có thể cung cấp oxy và chất dinh dưỡng đến khối u, cho phép nó phát triển. Bevacizumab thường được sử dụng kết hợp với hóa trị liệu và được chỉ định khi ung thư phổi muộn và tái phát không phải tế bào nhỏ. Bevacizumab có nguy cơ gây chảy máu, rối loạn đông máu và huyết áp cao.
- Erlotinib (Tarceva). Erlotinib, tác động đến tế bào ung thư phát triển và phân chia. Erlotinib được dùng cho những bệnh nhân ung thư mới và tái phát ung thư phổi không phải tế bào nhỏ mà hóa trị không kết quả. Tác dụng phụ bao gồm phát ban trên da và tiêu chảy.
4.5. Chăm sóc giảm nhẹ
Khi điều trị có rất ít cơ hội chữa khỏi bệnh, có thể tránh điều trị và lựa chọn phương pháp chăm sóc giảm nhẹ thay thế. Nếu được chăm sóc hỗ trợ, có thể điều trị triệu chứng để làm cho bệnh nhân cảm thấy thoải mái hơn. Hỗ trợ chăm sóc cho phép tận dụng tối đa tuần hoặc tháng cuối cùng mà không có tác dụng phụ tiêu cực có thể tác động đến chất lượng sống.
Phương pháp phòng bệnh là tránh các tác nhân nguy cơ như khói thuốc và không khí ô nhiễm.
Bệnh viện Nguyễn Tri Phương - Đa khoa Hạng I Thành phố Hồ Chí Minh






