️ Hướng dẫn chẩn đoán và điều trị ung thư tuyến tiền liệt (P2)
Chỉ định can thiệp phẫu thuật
Chỉ định phẫu thuật theo loại kỹ thuật và đường tiếp cận tuyến tiền liệt
Phẫu thuật mở hay nội soi có cùng chỉ định như nhau, việc quyết định phương pháp nào là tùy thuộc sự lựa chọn và kinh nghiệm của phẫu thuật viên.
Riêng với đường mổ qua vùng đáy chậu nên được khuyến khích cho ung thư giai đoạn khu trú, vì cho kết quả tốt và đảm bảo thẩm mỹ. Tuy nhiên, khi lựa chọn đường mổ này cần phải xác định là: không có di căn hạch, với các tiêu chuẩn kèm theo là PSA<10ng/ml, Gleason <7, tốt nhất là có sinh thiết hạch chậu âm tính.
Chỉ định theo bệnh lý
Căn cứ vào giai đoạn bệnh
Theo độ mô bệnh học.
Theo thời gian kỳ vọng sống thêm.
Theo tình trạng của các bệnh kèm theo của người cao tuổi như: bệnh tim mạch, bệnh đái tháo đường, di chứng tai biến mạch máu, bệnh của hệ thần kinh...
Xạ trị
Nguyên tắc xạ trị
Chỉ định xạ trị phụ thuộc vào:
Nguy cơ tái phát.
Thời gian kỳ vọng sống thêm.
Mục đích là điều trị triệt căn hay điều trị giảm nhẹ - Không đủ điều kiện sức khỏe để phẫu thuật - Nguyện vọng của người bệnh.
Kỹ thuật xạ trị
Kỹ thuật: 3 D-CRT, IMRT (Intensity Modulated Radiation Therapy- xạ trị điều biến liều), VMAT (xạ trị điều biến thể tích), IGRT (xạ trị dưới hướng dẫn hình ảnh)
Thiết bị: máy gia tốc tuyến tính
Liều lượng:
Nguy cơ thấp: 70Gy-75Gy trong 36-41 buổi vào tuyến tiền liệt ± túi tinh. Không xạ trị tiểu khung
Nguy cơ trung bình: 75- 80Gy. Phân liều 1,8-2,0Gy/lần, có thể xạ trị hạch chậu.
Nguy cơ cao: xạ trị hạch chậu
Có thể kết hợp xạ trị chiếu ngoài với xạ trị áp sát suất liều cao nạp nguồn sau.
Xạ trị chiếu ngoài vào vùng chậu
Chỉ định:
U giai đoạn T4.
Di căn hạch chậu.
Túi tinh bị xâm lấn.
Người bệnh thuộc nhóm nguy cơ cao.
Nguy cơ di căn hạch > 15%, tính theo công thức Roach:
Nguy cơ di căn hạch = (2/3) × PSA + [(GS – 6) × 10]
Hai trường chiếu trước-sau và sau-trước:
Giới hạn trên: khe giữa L5-S1.
Nếu hạch chậu (+): khe giữa L4-L5.
Giới hạn dưới: dưới hai ụ ngồi.
Giới hạn hai bên: 1-1,5 cm phía ngoài của khung chậu bé (che chắn đầu xương đùi và cánh chậu).
Trường chiếu hai bên:
Giới hạn trên và dưới: giống như của trường chiếu trước-sau.
Giới hạn trước: phía trước của khớp mu.
Giới hạn sau: đi qua khe S2-S3.
Xạ trị khu trú vào tuyến tiền liệt
Chỉ định:
U giai đoạn sớm (T1, T2).
Hạch chậu (-).
Túi tinh không bị xâm lấn.
Nguy cơ di căn hạch < 15%, tính theo công thức Roach.
Người bệnh thuộc nhóm nguy cơ thấp đến trung bình.
Người bệnh thuộc nhóm nguy cơ cao, kèm điều trị nội tiết dài hạn.
Phối hợp liệu pháp ức chế androgen (ADT) ở ung thư tuyến tiền liệt di căn còn nhạy nội tiết nhóm nguy cơ thấp (di căn xương dưới 4 tổn thương, không di căn tạng)
Để xạ trị khu trú vào tuyến tiền liệt, có thể sử dụng các kỹ thuật xạ trị phù hợp:
Xạ trị chiếu ngoài (EBRT): kỹ thuật xạ trị 3D CRT (3D Conformal Radiotherapy); Xạ trị điều biến liều (IMRT), Xạ trị điều biến liều thể tích (VMAT), xạ dưới hướng dẫn hình ảnh (IGRT).
Xạ trị mô phỏng PET/CT hoặc CT
Xạ trị áp sát liều cao (HDR), cấy hạt phóng xạ vào mô tuyến tiền liệt để điều trị triệt căn UTTTL giai đoạn khu trú hoặc để nâng liều xạ sau xạ trị từ ngoài (xạ trị chiếu ngoài).
Tư thế nằm của người bệnh khi mô phỏng và xạ trị:
Người bệnh thường nằm ngửa, kê gối dưới khoeo chân. Đây là tư thế nằm thoải mái nhất.
Cũng có thể cho người bệnh nằm sấp để ruột non được đẩy lên trên, ra ngoài vùng chiếu xạ.
Nên cho người bệnh uống nước nhiều trước khi mô phỏng và xạ trị để làm căng bàng quang.
Khi mô phỏng nên tiêm tĩnh mạch một lượng nhỏ chất cản quang (40-50ml) để thấy rõ bàng quang và dễ phân biệt đáy tuyến tiền liệt với cổ bàng quang.
Xác định các thể tích xạ khi dùng kỹ thuật xạ trị phù hợp mô đích:
GTV (Gross tumor volume – Thể tích u thô): thường không sử dụng trong xạ trị
UTTTL, vì khó nhìn thấy nhân ung thư trong mô tuyến trên CLVT. Thể tích thường dùng là CTV.
CTV (Clinical target volume – Thể tích đích lâm sàng): toàn bộ tuyến tiền liệt (thường bao gồm 1/3 thể tích túi tinh) ± túi tinh (nếu túi tinh bị xâm lấn). - BTV (biologic target volume) là thể tích đích sinh học ảnh thu được từ chụp PET/CT mô phỏng để xác định thể tích
PTV (Planning target volume – Thể tích đích theo kế hoạch): CTV + 1cm về mọi hướng ngoại trừ hướng ra phía sau chỉ là 8 mm.
Liều xạ tối đa trên các cơ quan quan trọng:
Trực tràng:
Dưới 5-10% xảy ra độc tính độ III-IV trên trực tràng nếu
V50 (thể tích trực tràng nhận liều > 50 Gy) là 60-65%
V60 (thể tích trực tràng nhận liều > 60 Gy) là 45-50%
V70 (thể tích trực tràng nhận liều > 70 Gy) là 25-30%
Bàng quang:
Toàn bộ bàng quang: < 65 Gy.
Một phần nhỏ bàng quang: 75-80 Gy. Không quá 3% thể tích bàng quang nhận liều > 78 Gy.
Đầu xương đùi: liều trung bình < 50 Gy.
Liều xạ và mức năng lượng chùm tia
Phân liều mỗi ngày: 1,8 – 2Gy.
Chọn năng lượng chùm tia tùy vào độ dày của bụng người bệnh. Thường dùng tia X mức năng lượng 6-18 MV của máy xạ trị gia tốc thẳng.
Xạ vào vùng chậu (khi có chỉ định): 45-50 Gy.
Sau đó xạ khu trú vào tuyến tiền liệt (± túi tinh) cho đến 70-76Gy.
Xạ triệt để khu trú vào tuyến tiền liệt: 70-76 Gy.
Xạ vào nền tuyến tiền liệt sau phẫu thuật cắt tuyến tiền liệt tận gốc:
64-66 Gy nếu còn sót u vi thể.
≥ 70 Gy nếu còn sót u đại thể.
Với các kỹ thuật xạ trị mới như IMRT (Intensity modulated radiotherapy - Xạ trị điều biến liều), IGRT (Image guided radiotherapy – Xạ trị dưới hướng dẫn hình ảnh) có thể cho phép nâng liều xạ tại tuyến tiền liệt lên đến 80 Gy.
Xạ trị áp sát: có thể dùng kỹ thuật nạp nguồn sau suất liều cao (High dose rate afterloading brachytherapy) hoặc kỹ thuật cấy lưu các hạt iod phóng xạ (Iodine 125) vào tuyến tiền liệt.
Cấy hạt phóng xạ điều trị áp sát
Chỉ định
Nguy cơ thấp: cấy hạt phóng xạ điều trị áp sát đơn thuần
Nguy cơ trung bình: cấy hạt phóng xạ điều trị áp sát + xạ trị chiếu ngoài (40-50Gy) ± nội tiết (4-6 tháng).
Liều xạ trị:
Cấy hạt phóng xạ với I-125 liều 145Gy nếu với Pd-103 liều 125Gy.
Cấy hạt phóng xạ sau khi xạ trị chiếu ngoài 40-50Gy: với I-125 liều 110Gy và Pd-103 liều 100Gy.
Kỹ thuật cấy hạt phóng xạ vào khối u để điều trị ung thư tuyến tiền liệt, là sự cải tiến của xạ trị áp sát kết hợp với xạ trị chiếu trong đã được nhiều nước trên thế giới nghiên cứu áp dụng và đem lại nhiều lợi ích to lớn cho bệnh nhân. Hiện nay tại các nước phát triển như Hoa Kỳ, Đức, Nhật Bản, áp dụng cho ung thư tuyến tiền liệt giai đoạn sớm, khu trú.
Cấy hạt phóng xạ điều trị UTTTL là phương pháp xạ trị đưa các hạt phóng xạ I-125 kích thước nhỏ 4,5x0,8 mm phát tia gamma năng lượng thấp (35 keV), vào trong tổ chức khối u, có tác dụng tiêu diệt tế bào ung thư tại chỗ mà không hoặc ảnh hưởng rất ít tới mô lành xung quanh. Bức xạ gamma mềm của I-125 chỉ phát huy hiệu quả điều trị trong phạm vi vài milimet (mm) của các mô bệnh và không hoặc rất ít gây tổn thương các mô lành xung quanh. Ưu điểm nổi bật của kỹ thuật này là tạo ra liều hấp thụ bức xạ cao tại khối u, trong khi cơ quan và tế bào lành chỉ phải chịu liều bức xạ rất thấp. Các hạt phóng xạ có thời gian bán rã không quá ngắn và không quá dài (chẳng hạn với I-125 là 60 ngày) nên có thể để lại các hạt phóng xạ trong lòng tuyến tiền liệt mà không cần lấy ra sau khi cấy hạt phóng xạ vào. Dưới hướng dẫn của hình ảnh siêu âm, các kim chứa hạt phóng xạ này sẽ được đâm xuyên qua da ở vùng tầng sinh môn để đưa thẳng vào trong lòng của tuyến tiền liệt. Các hạt I-125 sẽ được lưu lại trong lòng tuyến tiền liệt sau khi kim được rút ra.
Ưu điểm của phương pháp cấy hạt phóng xạ là kiểm soát u tại chỗ cao, thời gian và liệu trình điều trị ngắn, ít biến chứng, chức năng sinh lý của nam giới (liệt dương) ít hoặc không bị ảnh hưởng, tăng chất lượng cuộc sống
Cấy hạt phóng xạ là một phương pháp điều trị an toàn, hiệu quả, tăng thời gian sống thêm, tăng chất lượng cuộc sống cho bệnh nhân ung thư tuyến tiền liệt giai đoạn sớm
Điều trị thuốc phóng xạ 177Lu-PSMA:
PSMA (prostate-specific membrane antigen) là protein xuyên màng, hay gặp ở màng tế bào ung thư tuyến tiền liệt. Đồng vị phóng xạ Lutetium-177 gắn với PSMA phát tia beta (E=490keV) và quãng chạy trong mô tuyến <2mm, thời gian bán rã 6,73 ngày. Thuốc phóng xạ 177Lu-PSMA sau khi đưa vào cơ thể sẽ tập trung tại các tế bào ung thư tuyến tiền liệt và phát tia bức xạ tiêu diệt khối u. Trước điều trị người bệnh được chụp 68Ga-PSMA PET/CT để đánh giá các tổn thương di căn và dự báo đáp ứng điều trị. Liều thuốc 177Lu-PSMA: 3,5-8GBq, tiêm tĩnh mạch chậm, 4-6 chu kỳ, mỗi chu kỳ 6 tuần.
Liệu pháp ức chế Androgen
Điều trị giai đoạn di căn
Liệu pháp ức chế Androgen (Androgen deprivation therapy - ADT) đóng vai trò cơ bản trong điều trị UTTTL di căn.
Cắt tinh hoàn ngoại khoa hay cắt tinh hoàn nội khoa bằng các thuốc đồng vận thụ thể GnRH (Gosereline, Triptoreline, Leuprorelin acetate) hoặc đối vận (Degarelix) cho hiệu quả tương đương.
Thuốc đối vận thụ thể GnRH làm giảm nhanh Testosterone trong máu ở những tuần đầu, không gây cơn cường phát bệnh, được ưu tiên cho các trường hợp di căn xương có chèn ép tủy, và các trường có triệu chứng rầm rộ cần kiểm soát nhanh.
Một số phác đồ điều trị nội tiết hiện có:
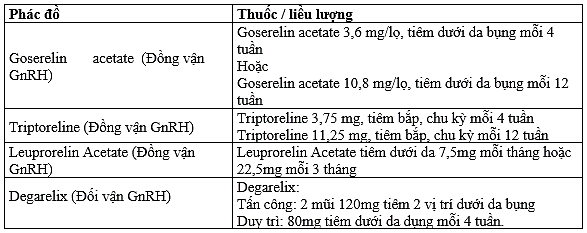
Liệu pháp nội tiết kết hợp bao gồm cắt tinh hoàn (nội hoặc ngoại khoa) và thuốc kháng Androgen (Antiandrogen) cho hiệu quả không hoặc ít cải thiện so với cắt tinh hoàn đơn thuần nên cân nhắc khi sử dụng thường quy.
Những trường hợp có nguy cơ bùng phát mạnh các triệu chứng khi sử dụng đồng vận GnRH cần phải được điều trị trước bằng kháng Androgen ít nhất 7 ngày.
Điều trị ngắt quãng không thể kết luận được rằng cho kết quả về sống còn toàn bộ không kém hơn điều trị liên tục ở người bệnh UTTTL di căn. Chính vì vậy không khuyến cáo điều trị ngắt quãng cho UTTTL di căn, trừ trường hợp có nhiều tác dụng không mong muốn và PSA đạt gần triệt tiêu với ADT. Những trường hợp điều trị ngắt quãng cần phải giải thích kỹ với người bệnh.
Hiệu quả của hóa trị Docetaxel kết hợp với ADT trong điều trị ngay từ đầu UTTTL di căn được chỉ ra trong hai thử nghiệm lâm sàng pha 3. Kết quả cho thấy nhóm điều trị kết hợp có cải thiện sống thêm so với ADT. Khác biệt rõ rệt ở nhóm người bệnh có nguy cơ cao, được xác định là có di căn tạng hoặc có ít nhất 4 tổn thương xương và trong đó có ít nhất 1 tổn thương ngoài khung chậu, cột sống. Do vậy, điều trị kết hợp Docetaxel – ADT nên được cân nhắc ngay từ đầu cho những trường hợp UTTTL di căn có nguy cơ cao và thể trạng cho phép.
Kết hợp Abiraterone acetate với ADT cải thiện sống còn toàn bộ và sống không bệnh tiến triển trên hình ảnh so với ADT ở nhóm người bệnh có nguy cơ cao (có 2 trong 3 yếu tố sau: điểm gleason ≥ 8, ít nhất 3 ổ tổn thương xương, di căn tạng). Tháng 2/2018, chỉ định điều trị phối hợp abiraterone acetate với ADT cho UTTTL còn nhạy với điều trị cắt tinh hoàn được chấp thuận bởi Cục quản lý Thực phẩm và Dược phẩm Hoa Kỳ (Food and Drug Administration - FDA). Liều khuyến cáo là Abiraterone acetate 4 viên/ngày kết hợp với prednisolon 5mg/ngày.
Điều trị phối hợp
Điều trị bổ trợ trước cho phẫu thuật triệt căn không có nhiều lợi ích, là chỉ định chưa rõ ràng.
Trong một thử nghiệm ngẫu nhiên, ở người bệnh di căn hạch sau phẫu thuật cắt TTL triệt căn, điều trị ADT sớm và liên tục cải thiện sống thêm so với nhóm trì hoãn ADT.
Điều trị bổ trợ trước, đồng thời hoặc bổ trợ cho xạ trị triệt căn cải thiện thời gian sống thêm.
Tiến triển sinh học
Người bệnh tăng PSA đơn thuần sau phẫu thuật hoặc xạ trị triệt căn được gọi là tiến triển sinh học
Chỉ định điều trị ADT tuỳ trường hợp cụ thể
Nếu thời gian tăng gấp đôi của PSA dưới 12 tháng, sống thêm ước tính trên 15 năm, nên điều trị ADT sớm.
Nếu thời gian tăng gấp đôi PSA dài trên 12 tháng, người bệnh tuổi cao, nhiều bệnh lý phối hợp thì nên theo dõi.
Nếu quyết định điều trị ADT thì điều trị ngắt quãng để giảm tác dụng không mong muốn của điều trị.
Các điều trị nội tiết khác
Kháng androgen
Kháng Androgen loại Steroid:
Cyproterone acetate, Megesterone acetate, Medroxyprogesterone acetate. Tác dụng phụ cần chú ý trên hệ tim mạch và chức năng gan. Ngày nay ít được sử dụng do vì không có hiệu quả khi điều trị kết hợp với liệu pháp cắt tinh hoàn.
Kháng Androgen không steroid:
Bicalutamide: 1 lần trong ngày, 50 mg/ngày
Các thuốc kháng androgen khác như: Flutamide, nilutamide.
Ức chế tổng hợp nội tiết nam
Aminoglutethimide: liều 1000mg/ngày; ức chế tổng hợp testosterone qua ức chế chuyển hóa cholesterol thành pregnenolone; hiện chỉ được sử dụng trong ung thư giai đoạn kháng cắt tinh hoàn, chỉ định ngày càng hạn chế.
Ketoconazol: liều 300 mg, 3 lần mỗi ngày; ức chế tổng hợp testosterone và cả steroid thượng thận; tương tự như đối với aminoglutethimide, hiện chỉ được sử dụng trong ung thư giai đoạn kháng cắt tinh hoàn.
Các tác nhân nội tiết mới
Abiraterone Acetate
Thuốc ức chế không đảo ngược protein tổng hợp bởi gen CYP17 (bao gồm 17, 20lyase và 17-alpha-hydroxylase) qua đó ngăn cản sự tổng hợp androgen tại chính tế bào ung thư tuyến tiền liệt, tinh hoàn và thượng thận. Thuốc được dùng kết hợp với prednisone/prednisolone để giảm tác dụng không mong muốn. Thuốc được chỉ định chủ yếu ở giai đoạn kháng cắt tinh hoàn, liều khuyến cáo là uống 4 viên kết hợp với prednisolone 10mg/ngày và ADT. Hai nghiên cứu pha III cho thấy phối hợp abiraterone/prednisone có hiệu quả tăng thời gian sống còn và cải thiện triệu chứng lâm sàng ở người bệnh đã hoặc chưa hóa trị trước với docetaxel.
Enzalutamide
Tác động trên nhiều vị trí của đường tổng hợp androgen: ngăn cản kết hợp androgen và thụ thể, ức chế chuyển vị và ngăn kết hợp với DNA của thụ thể androgen tại nhân tế bào. Thuốc có hiệu quả ở UTTTL kháng cắt tinh hoàn đã hoặc chưa hóa trị và/hoặc sử dụng phối hợp với ADT trong ung thư tuyến tiền liệt di căn còn nhạy với cắt tinh hoàn. Thuốc chống chỉ định cho người bệnh có tiền căn co giật dù tác dụng phụ này rất hiểm xảy ra (0,6%). Liều lượng enzalutamide 40mg x 4 viên/ngày.
Các thuốc khác như apalutamide, darolutamide đã được nghiên cứu chứng minh hiệu quả với ung thư tuyến tiền liệt kháng cắt tinh hoàn.
Hoá trị
Docetaxel:
Nghiên cứu pha III TAX 327 ghi nhận docetaxel 75mg/m2 mỗi 3 tuần phối hợp với prednisone 10mg/ngày có hiệu quả cải thiện thời gian sống còn hơn so với mitoxantrone/prednisone. Theo kết quả này, docetaxel/prednisone đã trở thành phối hợp tiêu chuẩn điều trị bước một UTTTL kháng cắt tinh hoàn.
Mitoxantrone:
Thuốc gây độc tế bào đầu tiên được chấp thuận cho UTTTL di căn với hiệu quả cải thiện triệu chứng lâm sàng. Hiện chỉ định thu hẹp cho những người bệnh có chỉ định hóa trị nhưng không dung nạp được taxane hoặc tiến triển sau taxan.
Cabazitaxel:
Một dẫn xuất taxane tổng hợp mới cho thấy có hiệu quả tăng thời gian sống còn khi phối hợp với prednisone điều trị người bệnh tiến triển sau docetaxel. Trong một nghiên cứu pha III, phối hợp cabazitaxel 25mg/m2 và prednisone cải thiện thời gian sống còn toàn bộ hơn 2,4 tháng so với mitoxantrone/prednisone. Tác dụng phụ chính là phản ứng tiêm truyền và độc tính tủy.
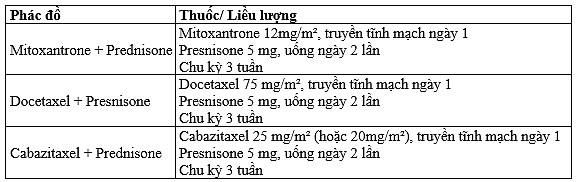
Thuốc chống hủy xương
Thuốc thuộc nhóm bisphosphonate, pamidronate, zoledrome acid có hiệu quả giảm triệu chứng và tần suất các biến cố liên quan di căn xương.
Denosumab: một kháng thể đơn dòng người có tác dụng ức chế chất kết nối RANK, qua đó ức chế hoạt động hủy cốt bào.
Điều trị miễn dịch
Thuốc ức chế chốt kiểm soát miễn dịch PD-1 như Pembrolizumab cũng bước đầu cho thấy có hiệu quả ở một nhóm người bệnh UTTTL di căn kháng cắt tinh hoàn và thất bại sau điều trị ít nhất một phương pháp và được FDA chấp thuận điều trị trên bệnh nhân có biểu hiện MSI-H hoặc dMMR sau khi thất bại với ít nhất một liệu pháp toàn thân trước đó.
Sipuleucel-T là vaccin cấu tạo bởi các tế bào có nhánh tạo ra từ các bạch cầu đơn nhân chiết xuất từ máu ngoại biên được gây đáp ứng miễn dịch với PAP (prostatic acid phosphatase) đã được chứng minh hiệu quả ở bệnh nhân UTTTL kháng cắt tinh hoàn sau điều trị Docetaxel.
Các thuốc ức chế PARP (Poly ADP ribose polymerase):
Olaparib: được chỉ định cho bệnh nhân ung thư tuyến tiền liệt kháng cắt tinh hoàn di căn có đột biến gen sửa chữa tái tổ hợp tương đồng dạng gây bệnh hoặc nghi ngờ gây bệnh tiến triển sau điều trị abiraterone acetate hoặc enzalutamide.
Dược chất phóng xạ:
Radium-223 là một dược chất phóng xạ phát ra bức xạ alpha. Radium có ái lực mạnh với mô xương bị tổn thương. Tại đây hiện tượng phân rã phóng xạ tạo ra các bức xạ năng lượng cao trong phạm vi ngắn hơn rất nhiều so với các đồng vị phát bức xạ beta. Điều này giúp tránh độc tính trên tủy xương và các cơ quan lân cận. Một nghiên cứu pha III cho thấy radium 223 có tính dung nạp cao, cải thiện thời gian sống còn toàn bộ và làm chậm thời gian xuất hiện các biến chứng liên quan di căn xương (nhu cầu xạ trị giảm đau, gẫy xương bệnh lý, chèn ép tủy, phẫu thuật chỉnh hình…). Chỉ định chủ yếu điều trị triệu chứng cho người bệnh UTTTL di căn xương không có các tổn thương nội tạng quan trọng.
Chăm sóc giảm nhẹ
Nguyên tắc điều trị giảm nhẹ cho UTTTL giai đoạn tiến xa là phối hợp đa mô thức gồm phẫu thuật giải phóng chèn ép, xạ trị giảm đau, xạ trị chống chèn ép, điều trị di căn, điều trị giảm đau, chăm sóc tâm lý…
Phẫu thuật
Phẫu thuật giải phóng chèn ép do khối u, hoặc do tổn thương di căn xa; phẫu thuật đưa niệu quản qua da, phẫu thuật dẫn lưu bàng quang
Xạ trị chiếu ngoài (EBRT)
Thiết bị: máy xạ trị gia tốc hoặc máy Cobalt-60.
Liều xạ trị: tùy theo vị trí di căn.
Di căn xương: xạ trị vào vị trí xương bị di căn liều 40Gy/20 buổi hoặc 30Gy/10 buổi hoặc 20Gy/5 buổi một số ít trường hợp xạ 1 liều 8Gy/1 buổi.
Di căn chèn ép tủy sống: xạ trị liều 30Gy/10 buổi.
Di căn gây chảy máu: xạ trị cầm máu khi các phương pháp nội khoa không hiệu quả liều 30Gy/10 buổi.
Di căn não: xạ toàn não hoặc xạ phẫu tùy trường hợp.
Xem tiếp: Hướng dẫn chẩn đoán và điều trị ung thư tuyến tiền liệt (P3)
Bệnh viện Nguyễn Tri Phương - Đa khoa Hạng I Thành phố Hồ Chí Minh






