️ Rickettsia Real-time PCR
MỤC ĐÍCH VÀ NGUYÊN LÝ
Mục đích
Phát hiện DNA của Rickettsia Real-time trong mẫu bệnh phẩm máu của người.
Nguyên lý
Phương pháp phát hiện dựa trên nguyên lý Real-time qPCR khuếch đại gen đặc hiệu của các loài vi khuẩn Rickettsia: Orientia tsutsugamushi và Rickettsia typhi.
CHUẨN BỊ
Người thực hiện
Người thực hiện: Nhân viên xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành Vi sinh (và/hoặc sinh học phân tử/ sinh học/công nghệ sinh học).
Người nhận định và phê duyệt kết quả: Người thực hiện có trình độ đại học hoặc sau đại học về chuyên ngành Vi sinh (và/hoặc sinh học phân tử/ sinh học/công nghệ sinh học).
Phương tiện, hóa chất (Ví dụ hoặc tương đương)
Trang thiết bị
Máy real-time PCR: Máy Real-time PCR có ít nhất 04 kênh màu và hệ thống máy vi tính (VD).
Máy tách chiết acid nucleic.
Bộ lưu điện.
Máy ở nhiệt.
Máy ly tâm dùng cho tube 0,2 ml
Máy ly tâm lạnh > 12000 gpm/phút
Tủ lạnh 20C -80C
Tủ âm sâu (-200 C) hoặc (-700C) (nếu có)
Máy vortex
Tủ an toàn sinh học
Micropipettes các thể tích từ 0,5 µl - 1000 µl.
Dụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm)
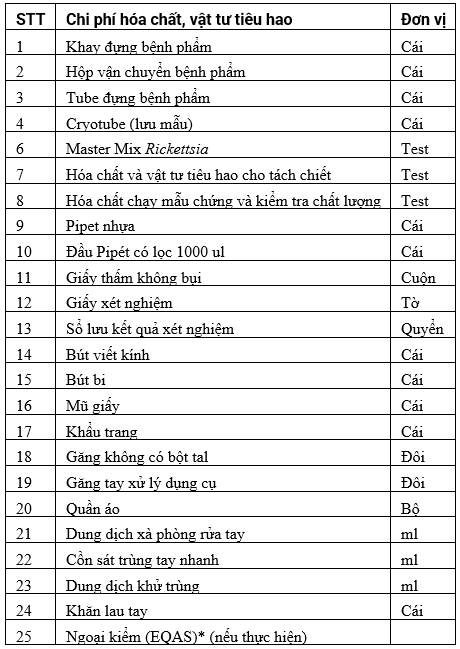
Ghi chú:
Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo Chương trình ngoại kiểm (EQAS) là 1/50 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 3 lần/1 năm).
Bệnh phẩm
Huyết tương tách từ máu có chất chống đông EDTA.
Phiếu xét nghiệm
Điền đầy đủ thông tin theo mẫu yêu cầu
CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên (VD sử dụng bộ sinh phẩm Rickettsia rPCR Mix hoặc sinh phẩm tương đương).
Lấy bệnh phẩm
Theo đúng quy định của chuyên ngành Vi sinh (Xem Phụ lục).
Tiến hành kỹ thuật
Phát hiện vi khuẩn Rickettsia bằng phản ứng Real-time PCR sử dụng Taqman probe.
Thu nhận và xử lý mẫu
Phải tách huyết tương trước khi tách chiết DNA.
Tách chiết DNA
Thực hiện phản ứng real-time PCR
NHẬN ĐỊNH KẾT QUẢ
Điều kiện của phản ứng
Kết quả chấp nhận được nếu cả 3 chứng đạt các điều kiện sau:
Chứng âm: không phát hiện.
Chứng dương: nằm trong khoảng cho phép c a nhà sản xuất (đ c hiệu với từng lô thuốc thử).
Chứng nội: với chứng âm và mẫu có nồng độ thấp (10-1000copies) phải có tín hiệu lên ứng với Ct khoảng 27 đến 30.
Ngược lại kết quả không được chấp nhận nếu không đáp ứng các điều kiện trên và phải thực hiện lại xét nghiệm:
Phân tích mẫu
Mẫu có tín hiệu FAM, ROX giá trị Ct ≤ 42 là mẫu dương tính với Orientia tsutsugamushi.
Mẫu có tín hiệu HEX, Cy5, ROX giá trị Ct ≤ 42 là mẫu dương tính với
Rickettsia typhi.
Mẫu có tín hiệu Cy5, ROX tín hiệu dương tính với các loài Rickettsia còn lại, không phải 2 loài Orientia tsutsugamushi và Rickettsia typhi.
Mẫu có tín hiệu FAM, HEX, Cy5 giá trị Ct > 42 là mẫu nghi ngờ nên cần tiến hành kiểm tra lại bằng phương pháp chạy điện di sản phẩm PCR, hoặc tách chiết lại DNA khuôn từ mẫu bệnh phẩm và chạy lại Real-time PCR để khẳng định kết quả.
Mẫu không có tín hiệu FAM, HEX, Cy5 và có tín hiệu ROX là mẫu âm tính
Mẫu không có tín hiệu FAM, HEX, Cy5, ROX là mẫu bị ức chế, cần tách chiết DNA (có bổ sung nội chuẩn vào mẫu khi tách chiết) và chạy lại Real-time PCR.
NHỮNG SAI SÓT VÀ XỬ TRÍ
Sự cố
Có mẫu và chứng nội cũng đ u âm tính. Chứng bình thường, có mẫu dương, mẫu âm thật sự.
Nguyên nhân
Có thể mẫu âm thực sự, có thể phản ứng PCR bị ức chế.
Khắc phục
Pha loãng mẫu từ 10-100 lần, thực hiện lại toàn bộ thí nghiệm từ bước tách chiết. Sau khi có kết quả phải nhân thêm với hệ số pha loãng mẫu.
Nếu vẫn gặp sự cố trên, lấy lại mẫu theo đúng yêu cầu.
Bệnh viện Nguyễn Tri Phương - Đa khoa Hạng I Thành phố Hồ Chí Minh






