️ Helicobacter Pylori nuôi cấy, định danh và kháng thuốc
MỤC ĐÍCH VÀ NGUYÊN LÝ
Mục đích:
Phát hiện, định danh và xác định mức độ nhạy cảm với kháng sinh của Helicobacter pylori bằng phương pháp nuôi cấy kinh điển.
Nguyên lý:
Sử dụng môi trường chọn lọc để phân lập, phát hiện vi khuẩn H. pylori.
Định danh dựa trên các đặc điểm nuôi cấy, một số tính chất chuyển hóa, các đặc điểm về hình thái học.
Thử nghiệm tính kháng thuốc của H. pylori bằng kỹ thuật kháng sinh đồ dải giấy khuếch tán theo bậc nồng độ.
CHUẨN BỊ
Người thực hiện:
Người thực hiện: Nhân viên xét nghiệm đã được đào tạo và có chứng chỉ hoặc chứng nhận về chuyên ngành vi sinh.
Người nhận định và phê duyệt kết quả: Người có trình độ đại học hoặc sau đại học về chuyên ngành vi sinh.
Phương tiện, hóa chất (Ví dụ hoặc tương đương):
Trang thiết bị:
.png)
ụng cụ, hóa chất và vật tư tiêu hao (bao gồm nội kiểm, ngoại kiểm):
Chi phí cho hóa chất và vật tư tiêu hao nuôi cấy, định danh vi khuẩn H. pylori:

Chi phí cho hóa chất và vật tư tiêu hao thử nghiệm kháng thuốc với vi khuẩn H. pylori:
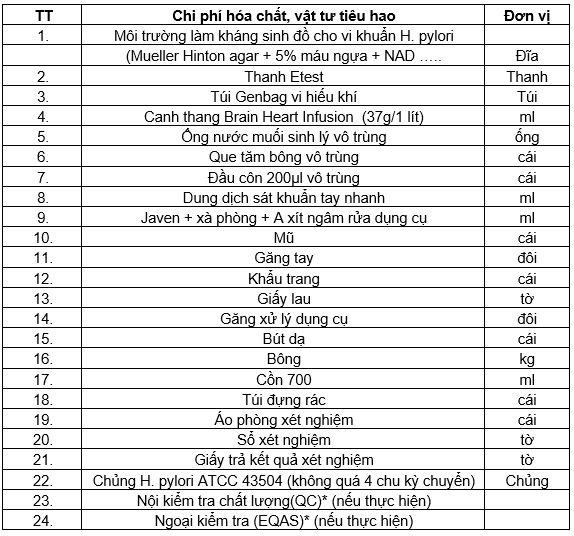
Ghi chú:
Chi phí nội kiểm cho quy trình kỹ thuật được tính cụ thể theo chương trình nội kiểm (QC) là 1/10 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lượng > 10 mẫu cho 1 lần tiến nhành kỹ thuật).
Chi phí ngoại kiểm cho quy trình kỹ thuật được tính cụ thể theo chương trình ngoại kiểm (EQAS) là 1/200 tổng chi phí dụng cụ, hóa chất, vật tư tiêu hao (với số lần ngoại kiểm trung bình 2 lần / 1 năm).
Bệnh phẩm:
Bệnh phẩm mảnh sinh thiết dạ dày qua ống nội soi.
Phiếu xét nghiệm:
Điền đầy đủ thông tin theo mẫu phiếu yêu cầu.
CÁC BƯỚC TIẾN HÀNH
Các bước tiến hành thực hiện theo phương tiện, hóa chất được ví dụ ở trên.
Lấy bệnh phẩm:
Theo đúng quy định của chuyên ngành vi sinh.
Lấy bệnh phẩm mảnh sinh thiết dạ dày qua ống nội soi.
Lấy ở vùng hang vị / thân vị dạ dày, tại các rìa ổ loét hoặc các vị trí có tổn thương nghi ngờ do H. pylori (trợt, niêm mạc sần,...).
Chuyển bệnh phẩm sinh thiết vào môi trường bảo quản, vận chuyển.
Môi trường vận chuyển có thể là nước muối sinh lý vô trùng nếu vận chuyển ngay về khoa xét nghiệm vi sinh (trong vòng 1h).
Nếu thời gian vận chuyển quá 1h giờ sau khi lấy mẫu, các mẫu sinh thiết phải được bảo quản trong môi trường Portagerm pylori, vận chuyển nhiệt độ (2025oC) tối đa 48h. Với các mẫu lưu trữ lâu dài, bảo quản ở -80oC trong môi trường chứa 30% glycerol.
Không nhận những mẫu bệnh phẩm đã ngâm trong dung dịch formalin.
Tiến hành kỹ thuật:
Nhuộm Gram và nuôi cấy:
Nghiền nát các mảnh sinh thiết bằng dụng cụ chuyên dụng hoặc dùng lớp cấy ria trực tiếp mảnh sinh thiết lên mặt đĩa thạch nếu thấy có nhiều nhầy của niêm mạc, phần còn lại dàn tiêu bản để nhuộm Gram.
Đặt đĩa thạch vào trong bình Jar có túi tạo môi trường vi hiếu khí, ủ ấm ở 35- 37oC, quan sát sau 3 đến 7 ngày.
Định danh:
Trên môi trường nuôi cấy, khuẩn lạc nghi ngờ H. pylori là những khuẩn lạc nhỏ, không màu ho c trong; Nhuộm Gram có hình cong, xoắn nhẹ, Gram âm; oxydase (+), catalase (+) và urease (+). Trường hợp vi khuẩn mọc ít cần cấy chuyển sang đĩa thạch mới để tăng sinh.
Thử nghiệm tính kháng thuốc:
Từ đĩa nuôi cấy có khuẩn lạc vi khuẩn H. pylori thuần khiết:
Tạo huyền dịch vi khuẩn nồng độ 3 McFarland trong canh thang Mueller Hinton + 5% huyết thanh ngựa hoặc canh thang BHI + 5% huyết thanh ngựa.
Sau khi ria đều vi khuẩn lên mặt thạch, chờ cho se mặt thạch, dùng panh đầu nhọn đặt Etest lên mặt thạch sao cho mặt có ghi dải nồng độ hướng lên trên và phải đảm bảo toàn bộ bề mặt của thanh Etest được tiếp xúc hoàn toàn với mặt thạch; đặt tối đa 1 thanh Etest trên đĩa 90mm.
Đặt đĩa thạch vào trong bình Jar có túi tạo môi trường vi hiếu khí, ủ ấm ở 35 - 37oC, 72 giờ.
NHẬN ĐỊNH KẾT QUẢ
Khuẩn lạc của H. pylori có đỉnh nhọn, mờ và khó nhìn do vậy khi đọc kháng sinh đồ phải nghiêng đĩa thạch và sử dụng ánh sáng xuyên để đọc điểm cắt của hình elip với thanh Etest; Phiên giải kết quả của thanh kháng sinh Etest theo EUCAST.
NHỮNG SAI SÓT VÀ XỬ TRÍ
Kiểm tra chất lượng:
Các loại dụng cụ, hóa chất, sinh phẩm, môi trường nuôi cấy phải còn hạn sử dụng và được kiểm tra chất lượng trước khi sử dụng.
Sử dụng chủng H. pylori ATCC 43504 để kiểm tra chất lượng.
An toàn:
Coi tất cả các bệnh phẩm được xem như là nguồn nhiễm, áp dụng các biện pháp an toàn đối với phòng xét nghiệm An toàn sinh học cấp II.
Lưu ý:
Nuôi cấy có thể âm tính giả nếu Người bệnh gần đây đã dùng các thuốc kháng sinh hoặc chất ức chế bơm Proton, nên dừng thuốc ức chế bơm Proton 2 tuần và thuốc kháng sinh 4 tuần trước khi nội soi để có kết quả chính xác.
Bệnh viện Nguyễn Tri Phương - Đa khoa Hạng I Thành phố Hồ Chí Minh






