️ Miễn dịch cơ bản ứng dụng trong huyết học -truyền máu (P2)
BỔ THỂ
Bổ thể là gi?
Bổ thể (viết tắt C’) là một chuỗi protein huyết tương - chủ yếu là protein dạng enzym có thể bị hoạt hoá tạo ra các sản phẩm quan trọng phá huỷ tế bào, vi trùng bằng con đường miễn dịch, có thể là miễn dịch đặc hiệu như phản ứng kháng nguyên - kháng thể chống hồng cầu nếu có mặt bổ thể sẽ làm tan hồng cầu... có thể là miễn dịch không đặc hiệu, các sản phẩm bổ thể sẽ làm tăng hiện tượng thực bào (phagocytosis) và ẩm bào (opsonization); bổ thể khi hoạt hoá có thể tạo ra nhiều yếu tố có hoạt tính sinh lý. làm tăng thấm màng tô' bào, giảm huyết áp, gây dị ứng...
Các thành phần của bổ thể
Bổ thể có 9 thành phần được ký hiệu từ Cl đến C9.
Cl có 3 protein quan trọng: Clq, Clr, Cls. Riêng Clq có tới 6 nhánh, chỉ khi có ít nhất hai nhánh gắn với phần Fc thì nó mới được hoạt hoá. Thí dụ với IgG thì cần có hai phân tử mối hoạt hoá được Clq (H.1.6). Sau khi Clq hoạt hoá, chúng sẽ hoạt hoá tiếp Clr, Cls tạo thành phức hợp C1 hoạt hoá: Clqrs.
C4: Clqrs sẽ hoạt hoá C4 tạo thành hai phân tử C4b và C4a. C4b sẽ tiếp tục hoạt hoá C2.
C2: Phức hợp C4bCl hoạt hoá C2 tạo thành hai sản phẩm: C2b và C2a.
C3 là thành phần trung gian giữa hai con đường hoạt hoá bổ thể. Khi hoạt hoá C3 tách ra hai thành phần: C3a và C3b. C3b tiếp tục tham gia vào dây truyền hoạt hoá bổ thể, còn C3a có tác dụng như một chất gây dị ứng. C3 được hoạt hoá bằng hai con đường: cổ điển và đường tắt (hình 1.7).
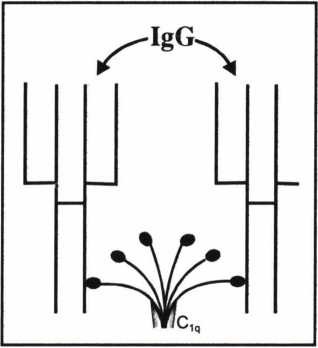
Hình 1.6. Hoạt hóa c1q bởi hai phân tử lgG.Clq có 6 đơn nguyên
gắn với phần Pc của phân tử kháng thể
C5: Khi bị hoạt hoá cũng có thể tách ra C5a và C5b. C5b tiếp tục hoạt hoá C6 và C7.
C6, C7, dưới tác dụng của C5b, hai thành phần này được hoạt hoá và tiếp tục tác động lên C8, C9.
C8, C9: hai thành phần cuối cùng bị hoạt hoá sẽ tạo ra các lỗ thủng làm thay đổi tính thấm màng tế bào, làm tế bào trương to và chết.
Các con dường hoạt hoá bổ thể
Bổ thể được hoạt hoá bởi hai con đường: đường cổ điển (classical pathvvay) và đường tắt (altemative pathvvay).
Đường cổ điển: đường hoạt hoá này là do phức hợp kháng nguyên + kháng thể, do các enzym (trypsin, plasmin, lysosozim), do endotoxin hoạt hóa với IgM, chỉ cần 1 phân tử IgM gồm có 5 đơn vị nhỏ (xem phần cấu trúc) là đủ để hoạt hoá bổ thể. Nhưng với IgG thì phải cần ít nhất là hai phân tử mới hoạt hoá được Clqrs. Các phân tử bổ thể hoạt hoá sẽ gắn vào phần Fc của phân tử khống thể. Sau khi Cls được hoạt hoá, chúng sẽ hoạt hoá tiếp C4 và C2 tạo thành ClC4bC2b. Phức hợp ClC4bC2b sẽ hoạt hoá tiếp C3. C3 có lượng lớn trong huyết thanh (khoảng 100 • 150mg/100ml) C3 hoạt hoá sẽ tạo nên phức hợp ClC4bC2bC3b, phức hợp này sẽ tiếp tục hoạt động trên con đường chung, bao gồm C5, 6, 7, 8, 9. .
Đường tắt: bằng đường này sự hoạt hoá bổ thể không cần sự có mặt của phức hợp MD (KN + KT). Các protein của đường tắt bắt đầu từ hoạt hoá C3. Các yếu tố có thể hoạt hoá C3 qua đường tắt là IgA, Zymozan, lipopolysaccharid, các khuẩn. Khi C3 được hoạt hoá sẽ tạo ra C3b, C3b cùng với yếu tố B đã được hoạt hoá bởi protease (yếu tố D) tạo thành phức hợp C3bBb, phức hợp này lại hoạt hoá tiếp C3 để tạo C3b. Đây là vòng hoạt hoá ngược (Feed-Back cycle) của C3 (H 1.7). Sự có mặt của C3b sẽ tiếp tục hoạt hoá C5, 6, 7, 8, 9 trên con đường chung.
Đường chung: sự có mặt của phức hợp ClC4bC2bC3b từ đường cổ điển và C3bBb sẽ hoạt hoá C5 tạo ra hai thành phần C5a và C5b. C5b sẽ tiếp tục hoạt hoá C6 C7 C8 C9. Toàn bộ phức hợp này sẽ gắn vào phần Fc của phân tử kháng thể trên bề mặt tế bào, làm thay đổi tính thấm màng tế bào, tạo các lỗ thủng ở màng tế bào, nước từ ngoài vào tế bào, tế bào trương to và bị phá võ.
Điều kiện thuận lợi cho phản ứng phá vỡ tế bào do C':
Nhiệt độ và pH thích hợp cho hoạt hoá các thành phần bổ thể. Nhiệt độ thường từ 32 - 37°c, pH thường là 6,8.
Khả năng hoạt hoá bổ thể của kháng thể: IgM mạnh hơn IgG vì IgM có nhiều vị trí gắn vối Clq hơn IgG.
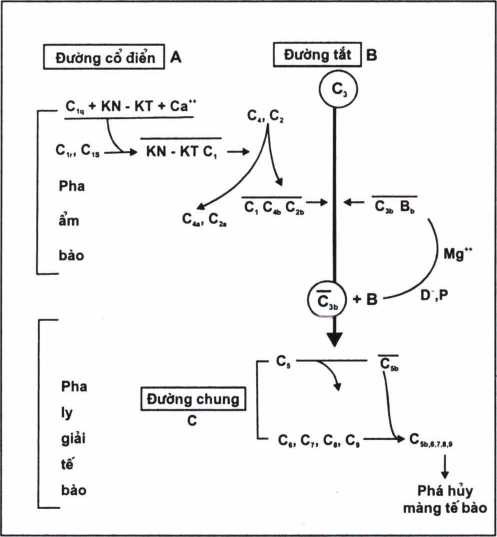
|
Hình 1.7. Sơ đồ hoạt hoá bổ thể theo: Đường cổ điển (A) Đường tắt (B) Đường chung (C) |
PHẢN ỨNG KHÁNG NGUYÊN, KHÁNG THỂ DỊCH THỂ
Phản ứng kháng nguyên + kháng thể dịch thể là phản ứng đặc hiệu giữa kháng thể là các Ig vối kháng nguyên đặc hiệu.
Để phát hiện phản ứng này có các kỹ thuật sau đây liên quan đến huyết học - truyền máu:
Kỹ thuật ngưng kết.
Kỹ thuật tan tế bào phụ thuộc bổ thể.
Phản ứng ngưng kết:
Phản ứng này có thể chia hai giai đoạn
Giai đoạn đầu: sự liên kết kháng nguyên + kháng thể Giai đoạn này có một sô yếu tô ảnh hưởng sau đây:
Tỷ lệ cân bằng kháng nguyên + kháng thể. Tỷ lệ này được tính theo công thức:
K1
(KN) + (KT) -------------- ► (KN - KT)
K2
K, và K2 là tỷ lệ cố định, có liên quan đến phản ứng KN + KT, liên quan với hằng số K
K1 (KN) (KT)
K =-------------------------- — =--- —--
K2 (KN) + (KT)
Khi K ở mức độ cân bằng thì phản ứng xảy ra rất mạnh, ngược lại thì phản ứng yếu không rõ ràng.
pH của môi trưòng phản ứng: trong khoảng từ 5,5 - 8,5.
Lực ion của dung dịch phản ứng.
Nhiệt độ: từ 37°c đến 40°c.
Giai đoạn thứ hai: ngưng kết thấy được, ở giai đoạn này hồng cầu kết dính với nhau tạo thành các mảng ngưng kết có thể thấy bằng mắt thường.
Kết quả của giai đoạn này phụ thuộc vào:
Mức độ tiếp xúc giữa tế bào và kháng thể: để tiếp xúc tốt có thể ly tâm, hoặc kéo dài thời gian ủ, hoặc bổ sung thêm albumin cho nhanh ngưng kết.
Điện tử tự do trên bề mặt hồng cầu: thường giữa các hồng cầu có khoảng cách khoảng 18nm, giữa các phân tử IgG trên bề mặt hồng cầu khoảng 12nm. Cho nên nếu có thêm chất bổ sung để rút ngắn khoảng cách này thì phản ứng xảy ra nhanh hơn. Mặt khác thường xung quanh hồng cầu có lớp áo khoác (coated layer), vì vậy phải tiêu huỷ chúng bằng protease (trypsin, papain) hoặc neuramidase.
Đời sống và hiệu lực của phân tử KT.
Vị trí và mật độ của nhóm quyết định kháng nguyên bề mặt hồng cầu.
Khả năng gắn bổ thể của phân tử KT
Phương pháp phát hiện phản ứng ngưng kết:
Phản ứng ngưng kết là phản ứng thường dùng nhất trong truyền máu, do KT đa hoá trị gắn với kháng nguyên trên bề mặt hồng cầu tạo thành mảng ngưng kết. Thường dùng các phản ứng sau:
Ngưng kết trực tiếp: thường do KT typ IgM - thường dùng kỹ thuật này xác định nhóm máu ABO.
Ngưng kết gián tiếp: ngoài kháng thể typ IgM, hầu hết KT nhóm máu ABO là typ IgG. Do số lượng vị trí gắn KT ít và khoảng cách xa (12nm) nên ngưng kết trực tiếp đôi khi khó khăn. Trong trường hợp này nếu được viện trợ thêm một số chất như protease, albumin, hoặc chất làm tăng kết dính như polybren thì phản ứng ngưng kết sẽ dễ dàng hơn.
Thử nghiệm bằng KT Coombs (Coombs test): sử dụng kháng thể kháng gammaglobulin, thử nghiệm Coombs dùng phát hiện các kháng thể thiếu (kháng thể không hoàn toàn).
Test Coombs trực tiếp, có thế’ phát hiện sự có mặt của KT không hoàn toàn trên bề mặt hồng cầu.
Test Coombs gián tiếp, có thể phát hiện kháng thể không hoàn toàn trong huyết thanh. Trong trường hợp này phải tiến hành hai bước:
Bước 1: ủ huyết thanh bệnh nhân với hồng cầu nhóm 0 trong 60 - 90 phút, rửa sạch (loại kháng thể thừa).
Bước 2: Bổ sung anti - gammaglobulin (Coombs serum) quan sát hiện tượng ngưng kết hồng cầu.
Dùng microplat: có thể định được 800 - 1.000 mẫu xét nghiệm/ngày; đây là máy định nhóm tự động.
Dùng microcolum: sử dụng định nhóm máu trong cột gel.
Sử dụng kỹ thuật sàng lọc kháng thể: trường hợp huyết thanh bệnh nhân có nhiều loại kháng thể chông hồng cầu khác nhau - như anti - A, c, E của hệ Rh, M, N, s... trường hợp này cần sử dụng các kỹ thuật sàng lọc, nhất là bệnh nhân truyền máu nhiều lần, như kỹ thuật xử lý máu, kỹ thuật polybren, ủ ở nhiệt độ 37°c, kỹ thuật cột gel...
Phản ứng kết hợp bổ thể
Phản ứng này thường dùng để phát hiện kháng thể chống bạch cầu, phản ứng tan hồng cầu (ít dùng).
Xem tiếp: Miễn dịch cơ bản ứng dụng trong huyết học -truyền máu (P3)
Bệnh viện Nguyễn Tri Phương - Đa khoa Hạng I Thành phố Hồ Chí Minh






